危険物第4類に分類される引火性液体は、化学工場やプラントで多く使われています。その燃焼は複雑な化学反応の連続で、安全に取り扱うためには燃焼の基本原理を理解することが欠かせません。
化学プラントの設備設計・プラント運転において、非常に重要な知識です。この内容を知らずして化学プラントの設計はできない、といっても良いくらいです。個々の内容は決して難しくはありませんが、知るべき知識の数が多いので習得に時間が掛かるのは仕方がないでしょう。
本記事では、危険物第4類の燃焼原理をわかりやすく解説し、燃焼の特徴や安全管理のポイントも合わせて紹介します。
この記事を読むことで、危険物第4類の燃焼がどう進むのかを具体的に理解でき、現場での安全対策や事故防止に役立つ知識が身につきます。燃焼の特徴や制御方法もわかりやすく解説するので、初心者から経験者まで幅広く役立つ内容です。
この記事は、危険物取扱者シリーズの一部です。
危険物乙4の勉強で押さえる物理化学:水・気体・三態の性質は化学プラントでこう使う
危険物乙4|消火設備を危険物製造所で適切に選択できるコツ
危険物取扱者試験が化学工場の機電系エンジニアにおススメな理由
引火性液体とは?化学プラントにおける危険物第4類の取り扱いポイント
燃焼の3要素
皆さん、物が燃えるってどういう条件があるか考えたことがありますか?
燃えるものがあれば燃える
火があると燃える
こう考えている人もいるでしょう。間違ってはいません。
しかし、物が燃えるためには3つの条件をクリアしていないといけません。
1つでは駄目です。
これを燃焼の3要素と言います。
燃焼の3要素は、以下の3つを指します。
- 可燃性物質
- 酸素
- 熱源
可燃性物質
可燃性物質とは燃える物です。
紙も家も人間の体も燃えます。全部可燃性物質です。
化学プラントでは多量の油が可燃物として認識されます。
物が燃えた時に怖いのは、財産が失われるという点に目が行きがちですが、化学プラントの場合は命や環境に大きな影響を与えます。
燃える物が異常に多いからです。
火災というレベルを越えて爆発に至ることも十分に考えられます。
とはいえ、化学プラントで可燃性物質を取り除くことは不可能です。
化学プラントを捨て去らない限りは不可能。
燃焼の3要素のうち、1つは絶対に除去できないわけですね。
酸素
酸素は支燃物と表現することもあります。
酸素がないと物は燃えません。
空気中には酸素があるので、当然燃える要因になります。
ところが酸素がない環境では、ほとんどの物質は燃えません。
酸素さえ遮断できれば、燃える確率はかなり下げることが可能。
化学プラントでは酸素を除去することが、火災爆発を防ぐための基本的な対策として徹底されます。
窒素を使って酸素を除去するという発想です。
一部の物質は周りに酸素が無くても勝手に燃えます。
これは物質内に酸素分がある場合です。
特殊なように見えますが、化学プラントでは意外と取り扱います。
つまり、酸素が取り除けたから問題なし!とは言えないわけです。
どうでもいいですけど、燃焼反応は酸化とほぼ同じ意味です。
酸化をして熱が膨大に出て炎が出る
そういう関係性です。
酸化は酸素と反応物が化合すること。
人間が呼吸をして酸素を取り入れないと死んでしまいまうため、酸素はありがたい存在ですが、物が燃えるという意味では、ありがたくありません。
そう考えると酸素って怖いですね。
熱源
熱源とは言葉とおり熱の源です。
可燃性物質と空気があっても、熱源が無いと物は燃えません。
熱源として真っ先に思いつくのが「火」
化学プラントでは溶接や電動機などの火花が、熱源の火にグループ分けします。
これは明らかに燃える源ですよね。
火にさえ注意していれば大丈夫でしょうか。
そうともいません。
熱源として大事なのは静電気
静電気が起きた時に、エネルギーが解放されます。
このエネルギーが熱源として十分に成立します。
目に見える「火」とは違い、静電気は目に見えない・気が付かないことが多いです。
日常生活ではいつ発生するか考えことがありませんよね。
ドアノブを触ったり・セーターを脱いだ時に初めて気が付きます。
それくらい身近にありながら、気が付きにくいものです。
だからこそ対策も難しく、気を使います。
酸素の性質
酸素の性質を見ていきましょう。
一般的な性質
まずは一般的な性質から
- 比重1.005
- 融点-218℃
- 沸点-183℃
- 無色
- 無臭
比重が空気より重たいというのは意外でしょうか?
空気は窒素:酸素=79%:21%で、
窒素が分子量28、酸素が分子量32ということからも、
窒素が軽く酸素が重いということは想像が付くでしょう。
化学プラントの機械エンジニアとしては融点は意識することはありませんが、沸点は知っていると良いことがあるでしょう。
窒素をPSAで生成する場合に、窒素と酸素の沸点差の話題がでます。
無色無臭であることは日常生活でも感じますよね。
限界酸素濃度
限界酸素濃度とは限界の酸素濃度です。
何の限界かというと、物が燃えるために必要な酸素濃度の限界です。
酸素濃度は空気中では21%ですね。
これは非常に大事。
可燃物は、酸素の割合を考えた時に、物が燃えるために必要な酸素濃度が限界酸素濃度です。
限界酸素濃度は可燃物の種類によって違います。
可燃性物質が燃えないようにするためには、何らかのガスで希釈して酸素濃度を下げないといけません。
希釈ガスによって限界酸素濃度が変わります。
可燃性物質の種類に対して、希釈ガスと限界酸素濃度の関係を見てみましょう。
| 可燃性ガス | 二酸化炭素 | 窒素 |
| 水素 | 5.9% | 5.0% |
| プロパン | 14.3% | 11.4% |
| エチレン | 11.7% | 10.0% |
| プロピレン | 14.1% | 11.5% |
| ベンゼン | 13.9% | 11.2% |
危険物乙4の範囲内では、二酸化炭素で希釈すると酸素濃度を4~5%以下にすることと言われます。
化学プラントでは窒素で系内を希釈することが普通ですので、酸素濃度が10%以下であれば問題ないことになります。
自主的に管理酸素濃度を下げている会社もあるでしょう。
例えば、窒素で酸素濃度を5%まで希釈すると、水素でも燃えるか燃えないかという世界ですね。
水素ならもっと酸素濃度を下げるでしょう。
この場合は、窒素置換も特殊な方法で行います。
物が燃焼する原理
突然ですが、物が燃焼する原理って考えたことがありますか?
危険物乙4でも大事なことですが、日常的に意識することは少ないでしょう。
気体の燃焼が基本です。
気体の燃焼
気体の燃焼を解説します。
先に、気体・液体・固体の燃えるモデルを示しています。
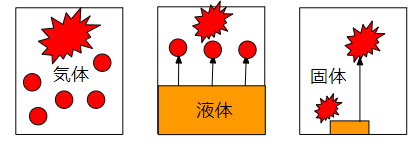
燃えるモデルがそれぞれ違うように見えますが、基本は気体の燃焼です。
気体は空気と接触して、可燃性ガスとなります。
この可燃性ガスが可燃物として定義されます。
可燃性ガスは気体と空気が混ざったものなので、気体と空気の割合が大事です。
気体の濃度が濃いと燃えて、薄いと燃えません。
下のようなイメージです。
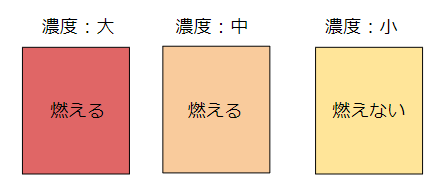
この限界点が限界酸素濃度と言いますね。
液体の燃焼
液体が燃えるってイメージしたことがありますか?
液体は実は燃えません。
液体が燃えるのではなくて、液体から蒸発した気体が燃えます。
液体は空気と接触すると必ず蒸発します。
下のようなイメージです。
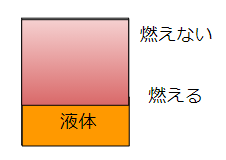
液体に近いほど蒸発した気体の濃度が高く、離れるほど濃度は低くなります。
この濃度が限界酸素濃度を越えたところで、物は燃えます。
液体が蒸発する量は温度で決まります。
温度が低い時は蒸発量はとても小さく、液体の表面でも物が燃えません。
液体の表面で可燃性ガスが燃焼範囲の限界となる温度を、引火点と言います。
引火点より低い温度では液体は燃えません。
引火点より高い温度だと液体表面や少し離れた場所でも可燃性ガスを形成して、燃えます。
これを蒸発燃焼と言います。
固体の燃焼
固体の燃焼って身近にありますよね。
木とか葉とか焚火をしたときに使いますよね。
これってどうやって燃えているでしょうか?
蒸発燃焼・表面燃焼・分解燃焼に分かれます。
蒸発燃焼
蒸発燃焼はレアケースです。
硫黄やナフタリンが例のようです。
危険物乙4受検者はその時だけ暗記していればいい世界です。
実務では私は扱ったことがありません。
表面燃焼
表面燃焼は、固体表面が高温になって酸素と反応して燃焼する現象です。
木炭やコークスが例です。
純粋に固体と酸素が反応する例です。
分解燃焼
分解燃焼は、固体表面が加熱されて分解したときに、可燃性ガスが発生して燃える現象です。
木材や石炭やプラスチックはこの例です。
温度が高くなると、割れたり溶けたりします。
ここで固体からガスが発生します。
ガスが発生すると気体と同じ扱いで可燃性ガスを形成して燃えます。
ニトロセルロースのように物質内に酸素を持っている分解燃焼は特に
自己燃焼や内部燃焼と言います。
物の燃えやすさ
燃えやすいと日常会話でも表現しますが、定義はあいまいです。
日常会話では、固体の燃焼だけが話題になるからです。
気体や液体も含めて考えると、もう少し掘り下げた定義が必要でしょう。
着火しやすい
「物の燃えやすさ」を指すときに真っ先に出るのが、この着火しやすさです。
ライターの火などを近づけたらすぐに燃えるものを「燃えやすい」といいますよね。
紙が良い例です。
ところが、紙は燃えた後すぐに燃え広がって消えますよね。
燃え続ける
「物の燃えやすさ」というとき、着火以外にも「燃え続ける」ということも重要な指標です。
木材とか炭が燃え続ける良い例でしょう。
その代わり、着火はしにくいですよね。
「着火のしやすさ」と「燃え続けやすさ」は同時に満足するとは限りません。
燃えやすさを示す特性
燃えやすさが「着火のしやすさ」と「燃え続けやすさ」に大きく分かれることは分かりました。
とはいえ、この区分に沿って燃えやすさを議論するのはあまり意味がありません。
「燃えやすい」というだけで化学プラントではすでにリスキーだからです。
そこで、燃えやすさを議論するときには、「着火のしやすさ」や「燃え続けやすさ」を区別しないで一般的な特性を使います。
全てが全て当てはまるわけではなく、一般的な傾向です。
酸化されやすいほど燃えやすい
酸化されやすいほど燃えやすいです。
これは化学反応を考えれば明らかです。
燃える = 酸化だからです。
燃えるとは物質が酸素と結合することそのものです。
そう考えると、酸化されやすいほど燃えやすいとは、当たり前のことを言っているだけです。
燃えやすいものほど燃えやすい、と言っているようなもの。
接触面積が大きいほど燃えやすい
接触面積が大きいものほど燃えやすいです。
これは酸素と結合する面積が広くなるからです。
固体だと表面積が広くなるので、液体よりも燃えやすくなりがちです。
面積が広いほど、燃え続けやすいという良い方もできます。
発熱量が大きいほど燃えやすい
発熱量が大きいものほど燃えやすいです。
熱が出るということは、その物が大きなエネルギーを持っているということです。
エネルギーを持っていると、エネルギーを発散させやすい傾向にあります。
着火しやすいわけではありませんが、燃え続けやすい傾向にあります。
熱伝導率が小さいほど燃えやすい
熱伝導率が小さいほど燃えやすいです。
熱伝導率が小さいということは、熱が溜まりやすいということです。
熱を周りに逃がせないと、燃え続けやすいといえるでしょう。
熱伝導率が小さい代表例である空気は燃えませんので、一般的な傾向という程度に留めてください。
水分が少ないほど燃えやすい
水分が少ないほど燃えやすいです。
これは直感的にも分かるでしょう。
湿っていると、水分を飛ばさない限り燃えませんよね。
固体でも水分を持っているか乾燥しているかで、燃えやすさは大きく変わります。
冬の乾燥している時の方が火事の危険が高いことが、一般的に知られていますよね。
可燃性蒸気が発生しやすいものほど燃えやすい
可燃性蒸気が発生しやすいものほど燃えやすいです。
液体が対象です。
危険物乙4の引火性液体がほぼほぼターゲットになります。
可燃性蒸気が発生しやすいとは、引火点が低いという表現で
化学プラントでは頻繁に使います。
これもよく考えれば、燃えやすいものほど燃えやすい、と言っているだけですよね・・・。
温度が高いほど燃えやすい
温度が高いほど燃えやすいです。
これも日常生活でイメージできるでしょう。
火が付いたら熱いですからね。
熱いものほど燃えやすいです。
これは引火性液体の引火点だけでなく発火点などとも関係します。
引火点と燃焼範囲
引火点と燃焼範囲について解説します。
プラントの安全性を考える上で、真っ先に考えることです。
引火点
引火点は以下の要素からなります。
- 空気中にある液体を点火して燃える
- 液体の液面上に可燃性ガスを作る
- 最低温度
引火点とは温度のことです。
液体を加熱していくと、蒸気になろうとします。
液面付近には液体の蒸気成分が濃い状態です。
液面から離れていくと、拡散してほぼ空気と見直せる濃度になります。
この意味で、引火点は蒸気圧と深い関係があります。
可燃性液体の温度が引火点より高い時は、引火する危険性があります。
この原則は非常に大事。
化学プラントのエンジニアなら誰もが知っておくべきことです。
燃焼範囲
燃焼範囲とは引火点を細かく見るときに登場します。
燃焼範囲のモデルを以下に示します。
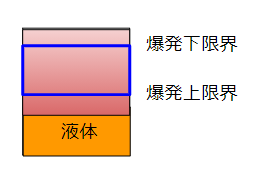
液体の表面には液体の成分が濃い気相が形成されます。
液体に近いほど濃く、遠いほど薄いです。
拡散されるということです。
拡散層とも言います。
液体が一定以上の温度になれば、液体の表面付近の空気中では液体成分の濃度は一定になります。
この一定の領域を飽和層とも言います。
燃焼範囲は、この可燃性蒸気のうち物が燃える範囲の濃度のことを言います。
範囲なので、濃度が上と下で囲まれた範囲です。
爆発上限界と爆発下限界という言い方をします。
液体に近い方が濃度が濃いので爆発上限界、遠い方が濃度が薄いので爆発下限界。
この範囲内にあれば、引火性液体は燃えます。
蛇足ですが、爆発上限界以上の濃度にある空気層は引火しません。
液体の表面直近だと必ず物が燃えやすい、というわけではありません。
現実的には液体の表面付近でも燃えるという前提で管理しますけどね^^
引火点と燃焼範囲の関係
引火点と燃焼範囲の関係を定性的に示しましょう。
液体の温度が高い時と低い時に燃焼範囲を以下に示します。
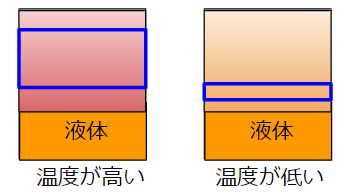
液体の温度が高い方が、液体成分が濃い空気層の範囲は広いです。
燃焼範囲にある空気層の領域が広いです。
液体の温度が低い方が、液体成分が含まれる空気層は狭くなり、燃焼範囲にある空気層の領域が狭くなります。
液体の温度が低い方が、燃焼範囲にある空気層は液体の表面側により近くなります。
液体の温度を下げていくと、燃焼範囲にある空気層の領域は徐々に小さくなり、最終的にはゼロになります。
この境目にある温度が引火点です。
燃焼範囲の具体的な値
燃焼範囲は、それぞれの物質に固有の値を持ちます。
当然ながら全部を覚える必要はなく、かといって全く知らないというわけにもいきません。
ここだけは理解したいというポイントを絞って紹介します。
水素 4~75%
水素の燃焼範囲は4~75%です。
これは機械系エンジニアも知っておくべきことです。
下一桁の値はどうでもいいです。
重要なのはこれ。
水素は最も燃焼範囲が広い
燃焼範囲が広いということは、どういうことでしょうか?
それだけ危険ということです。
化学プラントのプロセスエンジニアや製造部は当然これを理解しています。
窒素置換の方法も他の有機溶媒とは違う方法で行うでしょう。
私が働く工場では、置換回数を増やしていますね。
他の危険物とは違う目で見ています。
化学を知らない機械エンジニアに取ってみれば、
どんな物体にも固有の危険な特性があって、雨後の筍のようにポロポロと特別注意事項が出てくるから覚えられない。と諦める人もいます。
しかし、水素の燃焼範囲はそんな細かな話ではありません。
とっても大事。
危険物乙4でも登場するような、世間一般に知れ渡っている情報
という意味で基礎的な知識です。
化学について理解を深める時、自社の工場で取扱う物質を暗記するように眺めることも手の一つですが、
教科書レベルで常識となっている事項を抑えることも大事です。
トルエン 1.2~7.1%
トルエンの燃焼範囲は1.2~7.1%です。
この値を覚える必要はありませんが、知っておきたいことは以下のとおりです。
一般的な有機溶媒は10%以下
そんなに高い濃度でなくても危険ということがポイント。
空気中の酸素が21%なので、そこに1%程度の有機溶媒が混じるだけでも燃える
こう考えるとちょっとは怖くありませんか?
だからこそ、化学プラントの設備では酸素を極力排除しようとして、窒素置換をします。
この辺は専門的には三角図の話になりますが、省略します。
トルエンと同じように、ヘキサン・ベンゼン・ガソリンなども同じような燃焼範囲です。
なお、現場レベルでは限界酸素濃度の方が遥かに重要です。
というのも、酸素濃度計で窒素置換の良否を判断するためです。
アセトン 2.15~13.0%
アセトンの燃焼範囲は2.15~13.0%です。
これも具体的な値は覚える必要はありません。
一般的な有機溶媒よりも燃焼範囲がやや広い
これが大事です。
というのもアセトンは現場で頻繁に使うからです。
使い慣れていて安易に考えがちになるアセトンですが、意外と燃焼範囲が広く危険。
ということは是非とも抑えておきたいですね。
引火点と発火点の違い
引火点と発火点の違いについて紹介します。
この2つの単語は危険物乙4でとても大事な用語です。
名前が似ていて間違えやすいですよね。
化学プラントのエンジニアなら引火点になじみがあるので区別しやすいですが、初学者は戸惑うことでしょう。
定義も微妙に違います。
引火点と発火点の比較を紹介します。
| 項目 | 引火点 | 発火点 |
| 測定対象 | 液体・固体 | 気体・液体・固体 |
| 火源 | いる | いらない |
| 定義 | 空気中で火を近づけた時に 燃え出す最低温度 | 空気中で火を近づけずに 燃え出す最低温度 |
| ガソリン | -40℃以下 | 300℃ |
測定対象
測定対象が引火点と発火点で微妙に違います。
大事なのは引火点の方です。
引火点が対象となるのは液体と固体です。固体はおまけ。
気体には引火点はありません。
引火点が液体を対象にした特殊なものという認識の方が正しいでしょう。
引火性液体というくらい液体に特化した性質です。
一般にモノが燃えるという時、発火点の方がイメージしやすいでしょう。
これは気体・液体・固体すべてに適用できます。
火源
火源とは火種と読み替えてもいいでしょう。
引火点では火種が近くにないと燃えません。
火が無いから燃えない!って安心していると大間違い。
火種には静電気のように目に見えなくて、いつ発生するか分からないものもふくまれるからです。
発火点では火種が無くても燃えます。
これも火が近くになくても燃えるという意味で、いつ燃えるか分かりませんよね。
逆に考えてください。
いつ燃えるか分からない物体について、引火点や発火点という目に見える温度の形で物性を調査して、
人間が安全に扱えるようにしています。
温度
温度は引火点と発火点で明確に違います。
一般に発火点は引火点よりはるかに高いです。
引火点は範囲がさまざまありますが、常温近くに引火点を持つ物質もあります。
発火点はもっと高くて200℃~300℃以上の世界です。
バッチ系化学プラントでは200℃以上の温度で取り扱うことがないため、発火点は意識することがありません。
引火点は常温や零下もありえるので、日常生活で身近です。
特にガソリンは-40℃と、冬でも引火点より高い状態が維持されます。
ガソリンはどの時期に扱っても、燃える可能性がある
という意味ですね。こう考えると怖いですよ。
他の有機溶媒では、-40℃以上に引火点を持つ物質があり、
普通に使っている場合は、引火点を意識せず、静電気着火も意識しなくていいです。
こういう条件付きの物質とは違い、ガソリンは無条件で気を使う必要があります。
物質の危険性を示す指標
化学プラントでは大量の危険物乙4を取り扱いますので、危険性に関する専門用語は正しく理解しておきたいです。
機械エンジニアといえでも実務で活用します。
燃焼範囲
燃焼範囲は大きいほど、物質は危険と言えます。
燃焼範囲が大きい方が、可燃性蒸気が燃える可能性が高くなるからです。
それだけ取り扱いに注意が必要であるため、危険です。
蒸気圧
蒸気圧は大きいほど危険です。
蒸気圧が高いほど、液体から気体になろうとする力が大きいことを意味します。
蒸気圧は物質だけで決まらず、温度に依存します。
とはいえ同じ温度でも蒸気圧が高い方が危険。
常温でも蒸気圧が高い液体の方が気体になりやすいく、爆発性雰囲気を形成しやすいからです。
燃焼速度
燃焼速度は大きい方が危険です。
何となく当たり前に見えますよね。
ところで、燃焼速度の定義って何でしょうか?
爆発性雰囲気中を火炎が伝搬する速度のことを言います。
いったん燃え出して、どれだけ早く火炎が伝わるかという意味ですね。
映画やアニメで爆発が起きた時に、頑張って逃げようとするシーンがありますよね。
爆発の炎が広がっていくイメージとして認識しても良いでしょう。
逆に、伝搬速度が極めて小さいと、一瞬燃えてすぐに消えます。
燃焼熱
燃焼熱は大きいほど、危険です。
燃焼熱が大きいと燃えた時に発生する熱量が大きく、周囲の温度を上げるからです。
燃焼速度とも若干関係しますね。
燃焼熱が大きいと遠く離れた場所にも熱が伝わり、周囲の温度が上がったために発火する、という可能性もあります。
爆発下限界
爆発下限界は小さいほど危険です。
燃焼範囲が広いという解釈もできます。
爆発下限界が小さいということは、少しでも「その物」があれば燃えるということです。
同じ温度で同じ蒸気圧を持つ物質でも、爆発下限界が小さい方が燃えやすく危険。
最小着火エネルギー
最小着火エネルギーは小さいほど危険です。
最小着火エネルギーは着火爆発を起こすために必要な最小のエネルギー。
静電気による着火で、静電気が持つエネルギーの議論をするときに登場します。
電気伝導度
電気伝導度は小さいほど危険です。
電気伝導度が小さいと、静電気が帯電しやすいからですね。
静電気を溜めやすいと静電気放電が起きた時のエネルギーが大きくなります。
同じ最小着火エネルギーでも、電気伝導度が小さい物質ほど静電気放電のエネルギーが高いために危険。
電気伝導度が小さいと、熱伝導度も小さい方向であり危険です。
沸点
沸点は小さいほど危険です。
沸点は蒸気圧と密接な関係があります。
沸点は「蒸気圧が大気圧と等しくなる温度」のことですから。
比熱
比熱は小さいほど危険です。
比熱が小さいほど、同じ熱量でも温度上昇が大きくなります。
温度が高い方が、蒸気圧が高くなり、爆発性雰囲気を形成しやすくなるからです。
自然発火しやすい条件
まずは自然発火の機構について紹介します。
現象を理解するためには、区分が必要ですよね。
自然発火は主に以下の機構で発生します。
- 分解熱による発熱
- 酸化による発熱
- 吸着熱による発熱
- 微生物による発熱
いずれも発熱がキーワード。
自然界に放置していも反応が進み、発熱するために発火するというのが自然発熱の機構です。
自然発火の条件
自然発火の条件について説明します。
自然発火しやすい条件とは、熱が溜まりやすい条件と言えます。
上の項目で説明した通り、発熱がポイント。
自然状態で発熱をして、熱が溜まり続けることで発火点に到達するから、自然発火します。
ここで問題なのは、発熱量そのものよりも熱が溜まること。
熱が溜まりやすい状態は以下のとおりです。
- 熱伝導率が低い
- 物質が溜まっている
- 空気の流動が悪い
この条件は気体や液体よりも固体が対象となります。
熱伝導率が低いと、発熱が起きても熱を放散せずに溜め込み、温度上昇を起こします。
熱伝導率が低いとは物質そのものの熱伝導率だけを指しているのではありません。
粉末・繊維状のものだと、断熱性が非常にいいので、見かけの熱伝導率が下がります。
人間が衣服を着るのもこれと全く同じですよね。
物を堆積していると、熱伝導率が上がるのと同じ効果がありますね。
空気の流動が悪いことも、同じです。
空気は熱伝導率が低い物質ということがポイントですね。
熱の発生速度
自然発火をするためには熱の発生速度も問題になります。
熱の発生速度は「発熱量×反応速度」なので、発熱量と反応速度のそれぞれを確認する必要があります。
発熱量が大きい
発熱量は物質に固有です。
物によって変わるので、対策が取りにくいです。
反応速度が高い
反応速度が速い条件として、以下の条件があります。
- 温度
- 表面積
- 触媒
- 古い
- 新しい
温度は高い方が反応速度が速いです。
表面積は大きいほどが反応速度は速いです。
酸化をイメージすればいいですが、表面積が大きいほど酸素と接触する面積が多く、反応速度は速いといえるでしょう。
酸素と接触する機会が多いと、空気が流動しやすくなるので、熱が溜まりにくい側面はあります。
空気が流動しにくく、表面積が大きい物が危険であり、その意味で粉末や繊維が危険です。
触媒は反応を促進します。
乾性油に水を加えることもこの1つです。
油のしみたウエスを雨に晒していて、乾いた状態が続くことで発熱
というケースもあります。
古い物質は一般に反応が進んで不安定になっていると考えた方が良いでしょう。
古い油ほど分解しやすいです。腐るとも言います。
古い物質ほど分解しやすいので、反応しやすいということですね。
逆に新しい物質も危険です。これは例えば石炭。
発掘したばかりの新しい石炭は表面が酸化されていないので、発熱します。
古くても新しくても危ない、というのは管理が難しいですよね。
混合危険のパターン
混合危険とは言葉どおり「混ぜると危険」なもの。
トイレやお風呂場の洗剤にある「混ぜるな危険」。
まさに混合危険です。
混合危険は、混ぜるという点で組み合わせの話になります。
まずは、混合危険のパターンについて見ていきましょう。
酸化性物質と還元性物質
酸化性物質と還元性物質を混合すると危険です、
混合することで発熱が起こるからです。
酸化性物質は危険物第一類と第六類が該当します。
還元性物質は危険物第二類と第四類が該当します。
酸化性物質と還元性物質の組み合わせ例を紹介します。
- 塩素酸カリウム+赤りん
- 無水クロム酸+アルコール
- 発煙硝酸+アニリン
化学プラントの機電系エンジニアなら、何となく聞いたことがあるという程度の扱いで大丈夫です。
酸化性塩類と強酸
酸化性塩類と強酸も同じように危険です、
酸化性塩類とは塩素酸塩、過塩素酸塩、過マンガン酸塩などが該当します。
具体例を紹介します。
- 塩素酸カリウム+硫酸
- 過マンガン酸カリウム+硫酸
- 重クロム酸カリウム+硫酸
これも何となく知っているだけでOK
敏感な爆発性物質を作るもの
敏感な爆発性物質を作るものも危険です。
というか、この一般的な表現で全部包含してもいいのでは?
と化学プラントの機械エンジニアなら思っても当然です。
具体例を紹介します。
- アンモニア+塩素
- アンモニア+塩素酸カリウム
これら以外にも組み合わせはいっぱいあります。
ヘッダー
配管ヘッダーは異なる配管が集合する場所という良い方もできます。
ポンプヘッダーのように1つの液を異なる行先に分岐する物もありますが、タンクヘッダーなどは異なる2液が集合します。
バッチ系化学プラントでは多くの配管がヘッダーで集合します。
ここでヘッダーに混合危険物が集合すると危険です。
2液を接触させて反応する場合は、混合危険の1つとして考えます。
これを反応器内で接触させるか、ヘッダーで混合させるか、だけの違いになります。
しかしこれが大事。
ヘッダーでは冷却手段が無いからです。
ヘッダーで混合危険を起こすと、温度はどんどん上がっていきます。
多くの配管を使い分けるバッチ系化学プラントでは、ヘッダーで混合危険を起こさないような工夫が必要です。
切替配管
バッチ系化学プラントでは切替配管が多いです。
切替をする理由は、配管の一部を流用するためです。
ここで切替配管ならまだいいのですが、遮断板やバルブで仕切ろうとすると混合危険のリスクが発生します。
遮断板が割れていたり、バルブが内通するケースですね。
バッチ系化学プラントでは確実性を高めるために、切替配管が多いです。
混合危険を考えると切替配管は安心しますよね。
配管トレース
配管トレースも混合危険の対象となりえます。
危険なのは銅管トレースですね。
鉄パイプのトレースなら危険性は低いですが、銅はプロセス液と反応するケースがあります。
混合危険はプロセス液とだけ考えるケースが多いですが、設備内でも危険なパターンがあります。
見落としやすいですよ。
危険物の爆発の種類
「爆発」と言っても、消防法上は種類を分けています。
化学プラントの近くに住んでいる人は、「化学プラントは爆発する。怖い」というイメージが強いでしょう。
化学プラント内の事務系の人も全く同じ考え。
機電系エンジニアでも同じ考えの人がかなりの割合でいます。
爆発は怖い物であり、その怖さを強調して強調しすぎることはありませんからね。
ところが、爆発の種類を分類すると、少し違った目で見ることができます。
可燃性蒸気
可燃性液体の蒸気が、燃焼範囲にある時に爆発する可能性があります。
一般には先に燃焼が起きます。
燃焼範囲にある蒸気が非常に広い時に、燃焼が速く伝わって爆発という状態になります。
化学プラントではいたる場所で消防法危険物を扱うので、「化学プラントはどこでも危ない。爆発する。」という印象を持つでしょう。
危険場所は0種・1種・2種に限定されます。
2種場所の設定が難しいからこそ、どこでも危ないという認識を持ってしまいます。
ここで、思考をストップしている人が多いのが現実です。
化学プラントのエンジニアでも大半はこの思考。
粉じん爆発
粉じん爆発とは、可燃性物質が粉体となって空気中に浮遊している状態です。
可燃性蒸気と同じように粉じん爆発も燃焼範囲を持ちます。
粉じん爆発は、化学プラントでは粉体を取り扱う部分に限定されます。
原料の仕込みや製品の充填などです。
化学プラントでは粉じん爆発の発生場所が限定されているから、恐ろしさを感じにくいです。
可燃性蒸気に比べて軽く考えがち。
でも、粉じん爆発って日常生活でも起きる可能性があります。
小麦粉なんかでも起きる可能性があります。
これが粉じん爆発の恐ろしいところ。
気体
可燃性気体も可燃性液体の蒸気と同じように燃焼します。
可燃性気体の典型例は、水素やアセチレンガス。
水素は化学プラントの反応で使うことがあります。
アセチレンガスは溶接や溶断で使います。
可燃性気体の方が可燃性液体の蒸気の方が、燃焼速度は速く爆発しやすいです。
火薬
火薬としては危険物第一類や第五類が考えられます。
第一類は可燃性はありませんが分子内に酸素を持っているため、可燃物と混合すると爆発の危険性が高くなります。
第五類は可燃物であり分子内に酸素を持っている恐ろしいものです。
外部から着火源が無くても勝手に燃える可能性があります。
ニトロ化合物や硝酸エステルなどが第五類に該当します。
火薬の基材としても使用されます。
機械エンジニアも「ニトロ」「硝酸」などの単語には敏感になった方が良いです。
第四類よりも第五類の方が怖いという認識も正しいでしょう。
参考
忙しいけど勉強したいというあなたには、以下の講座がおすすめです。
関連記事
さらに知りたい方は、以下の記事をご覧ください。
最後に
危険物第4類の燃焼は、蒸気の発生と空気との混合による化学反応が基本です。燃焼原理の理解は、安全管理や火災・爆発防止に不可欠です。正しい知識をもって、適切な管理を行いましょう。
燃焼の三要素、燃焼の原理、物の燃えやすさ、引火点・燃焼範囲、発火点、危険性の指標、自然発火・混合危険・爆発
どれも機電系エンジニアとして知っておくべき大事な知識です。
化学プラントの設計・保全・運転などの悩みや疑問・質問などご自由にコメント欄に投稿してください。(コメント欄はこの記事の最下部です。)
*いただいたコメント全て拝見し、真剣に回答させていただきます。
この記事の内容を、あなたの職場・キャリアに合わせて整理したい方に技術・キャリア相談を行っています。海外プラント、製造管理、組織の病理、キャリア停滞など、あなたの状況に合わせて具体的にアドバイスします
→ 技術・キャリア相談はこちら
【著者:ねおにーーと】
化学プラントで20年以上、設計→製造→保全→企画まで一気通貫で経験したユーザー側エンジニア。 バッチプラントの設備・運転・トラブル対応を中心に、現場で本当に役立つ知識を発信しています。 → 詳しいプロフィールはこちら


コメント